Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
Initialising ...
 -ray irradiation
-ray irradiation古澤 和也*; 北 恵里香*; 佐伯 俊彦*; 長澤 尚胤; 西 則雄*; 土橋 敏明*
Journal of Biomaterials Science; Polymer Edition, 19(9), p.1159 - 1170, 2008/09
デオキシリボ核酸(DNA)は発ガン性物質をインターカーション吸着する働きがあることから、このDNAを不溶化することによって、天然高分子由来の環境浄化材料を開発することが可能となる。そこで、本研究では食品加工残渣の鮭白子DNAを選定し、多糖類誘導体やタンパク質にブレンド後、放射線橋かけしてハイブリッドゲルを創製し、得られたゲルのゲル分率,膨潤度を調べるとともに、発ガン物質のモデル物質であるアクリジルオレンジを用いて吸着特性を評価した。カルボキシメチルセルロース,ゼラチン,アルブミンを用いた場合に効率よく橋かけし、50kGy照射でゲル分率が60%以上になり、その吸水特性は約200倍であることを見いだした。10kGy照射して得られたゼラチン/DNAゲルのアクリジルオレンジの吸着量は、DNA無添加に比べて10倍以上(1.8 g/g)に増加し、環境浄化材料としての有用性を確認できた。
g/g)に増加し、環境浄化材料としての有用性を確認できた。
浅野 雅春; 吉田 勝; 大道 英樹; 真下 透*; 岡部 和彦*; 湯浅 久子*; 山中 英寿*; 森本 成紀*; 榊原 秀夫*
Biomaterials, 14(10), p.797 - 799, 1993/08
この論文は、熱、pH変化などに不安定な薬物の固定技術及びin vitroでの薬物放出特性を調べた最初の報告である。骨粗鬆病などの治療に広く用いられているカルシトニンは、皮下注射による投与時に激痛をともなうことが知られており、また長時間にわたっての投与が必要とされているとこから、50 C以下の温度で成形加工しやすい分子量2,000
C以下の温度で成形加工しやすい分子量2,000 4,400のポリ(DL-乳酸)に固定し、ポリマーを分解させながら薬物を放出させる試みを行った。その結果、固定化物からの薬物の放出性は、S-字型分解パターンをもつ分子量4,400のポリマー系が最も優れた性能を示し、24日間の実験期間を通して約14units/dayの一定した放出レベルを維持できることが分った。
4,400のポリ(DL-乳酸)に固定し、ポリマーを分解させながら薬物を放出させる試みを行った。その結果、固定化物からの薬物の放出性は、S-字型分解パターンをもつ分子量4,400のポリマー系が最も優れた性能を示し、24日間の実験期間を通して約14units/dayの一定した放出レベルを維持できることが分った。
浅野 雅春; 吉田 勝; 大道 英樹; 真下 透*; 岡部 和彦*; 湯浅 久子*; 山中 英寿*; 守本 成紀*; 榊原 秀夫*
Biomaterials, 14(10), p.797 - 799, 1993/00
被引用回数:22 パーセンタイル:73.33(Engineering, Biomedical)「薬物投与の最適化」を目的に、近年、薬物送達システム(DDS)の開発が活発に行われている。我々は、DDS用素材として、生体内で分解、吸収、代謝される機能をもつ生体分解型ポリマー材料の設計・合成を行い、埋入型DDS担体のin vivo性能評価を行っている。今回、骨粗鬆症治療薬として知られているウナギカルシトニンの類似化合物、[Asu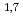 ]-ECT、を生体分解型ポリ(DL-乳酸)に圧融着法により包含した。1,400のMnをもつポリ(DL-乳酸)のin vitro分解パターンは放物線型であった。このポリマー複合体からの薬物のin vitro放出を調べたところ、初期段階で著るしく、3日で完了した。これに対し、Mnが4,400のポリマーの場合、分解パターンはS字型を示し、薬物のin vitro放出は24日間にわたって14
]-ECT、を生体分解型ポリ(DL-乳酸)に圧融着法により包含した。1,400のMnをもつポリ(DL-乳酸)のin vitro分解パターンは放物線型であった。このポリマー複合体からの薬物のin vitro放出を調べたところ、初期段階で著るしく、3日で完了した。これに対し、Mnが4,400のポリマーの場合、分解パターンはS字型を示し、薬物のin vitro放出は24日間にわたって14 5units/日の一定値を保つことが分った。
5units/日の一定値を保つことが分った。
福崎 裕延*; 吉田 勝; 浅野 雅春; 熊倉 稔; 真下 透*; 湯浅 久子*; 今井 強一*; 山中 英寿*
Biomaterials, 12, p.433 - 437, 1991/05
被引用回数:34 パーセンタイル:86(Engineering, Biomedical)16900~41300の重量平均分子量(Mw)をもつ無定形ポリ(L-ラクチド-Co-グリコライド、70:30mol%)を触媒の存在下開環重合によって調製した。この場合、分子量は分子量調節剤(ラウリルアルコール)を用いてコントロールした。このポリマーのin vivo分解パターンはS-型を示す。前立腺治療薬をMw=24000のポリマー中に包括し、in vivo分解とin vivo放出の関係を調べた。その結果、ポリマーからin vivoにおいて放出した薬物の累積放出量はポリマーの分解パターンとよく対応することが分かった。
福崎 裕延*; 吉田 勝; 浅野 雅春; 熊倉 稔; 真下 透*; 湯浅 久子*; 今井 強一*; 山中 英寿*
Biomaterials, 11, p.441 - 446, 1990/08
被引用回数:13 パーセンタイル:57.32(Engineering, Biomedical)70%L-乳酸(LA)を含む低分子量・無定形コポリエステルを種々のDL-オキシ酸(DL-LA:DL-乳酸、DL-HBA:DL- -ヒドロキシ-n-酪酸、DL-HIVA:DL-
-ヒドロキシ-n-酪酸、DL-HIVA:DL- -ヒドロキシ-iso-吉草酸、DL-HICA:DL-
-ヒドロキシ-iso-吉草酸、DL-HICA:DL- -ヒドロキシ-iso-カプロン酸)と無触媒下で直接脱水縮合させることにより合成した。ドラッグデリバリーシステムの生分解型担体としてのこれらのポリマーのin vivo性能は動物実験によって評価した。その結果、in vivo分解パターンは、担体の種類によって、放物線型(LA/DL-HBA)、直線型(LA/DL-LA)、そしてS-字型(LA/DL-HIVA、LA/DL-HICA)からなることが分かった。ポリマー複合体からの薬物の一定速度でのin vivo放出は、LA/DL-HICA系が最も効果的で、約15週の期間にわたって45
-ヒドロキシ-iso-カプロン酸)と無触媒下で直接脱水縮合させることにより合成した。ドラッグデリバリーシステムの生分解型担体としてのこれらのポリマーのin vivo性能は動物実験によって評価した。その結果、in vivo分解パターンは、担体の種類によって、放物線型(LA/DL-HBA)、直線型(LA/DL-LA)、そしてS-字型(LA/DL-HIVA、LA/DL-HICA)からなることが分かった。ポリマー複合体からの薬物の一定速度でのin vivo放出は、LA/DL-HICA系が最も効果的で、約15週の期間にわたって45 g/dayの速度で維持された。この効果は血中薬物濃度および薬理作用の結果から示唆された。
g/dayの速度で維持された。この効果は血中薬物濃度および薬理作用の結果から示唆された。
浅野 雅春; 福崎 裕延*; 吉田 勝; 熊倉 稔; 真下 透*; 湯浅 久子*; 今井 強一*; 山中 英寿*
Biomaterials, 10, p.569 - 573, 1989/10
被引用回数:37 パーセンタイル:92.86(Engineering, Biomedical)Mn=1800をもつ結晶・非晶性コポリマーをD-乳酸とL-乳酸の直接脱水共縮合によって合成した。このコポリマーは、主鎖にエステル結合をもつため、エステラーゼ酵素作用によって分解する。des-Gly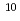 -(D-Leu
-(D-Leu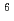 )-LH-RH ethylamideを、このコポリマー中に圧融着によって包含した。薬物のin vivo放出性は、コポリマーの結晶構造に強く依存し、結果的に非晶コポリマーからのin vivo放出が結晶コポリマーのそれより長期間にわたって調節可能であることが分った。逆に、担体自体のin vivo分解性は、非晶コポリマーの方がはやい。これは、薬物の分散状態の違いによって説明できる。すなわち、担体の分解は非晶部分から優先的におこるのに対し、薬物は結晶部分に分散していないためである。
)-LH-RH ethylamideを、このコポリマー中に圧融着によって包含した。薬物のin vivo放出性は、コポリマーの結晶構造に強く依存し、結果的に非晶コポリマーからのin vivo放出が結晶コポリマーのそれより長期間にわたって調節可能であることが分った。逆に、担体自体のin vivo分解性は、非晶コポリマーの方がはやい。これは、薬物の分散状態の違いによって説明できる。すなわち、担体の分解は非晶部分から優先的におこるのに対し、薬物は結晶部分に分散していないためである。
吉田 勝; 浅野 雅春; 森田 泰司*; 嘉悦 勲; 今井 強一*; 真下 透*; 湯浅 久子*; 山中 英寿*; 河原田 うめ子*; 鈴木 慶二*
Biomaterials, 10, p.16 - 22, 1989/01
被引用回数:10 パーセンタイル:45.97(Engineering, Biomedical)シスプラチンを低温放射線重合法によってビニルコポリマー(80/20vol-%組成のdiethylene glycol dimethacrylate/polyethylene glycol #600 dimethacrylate)中に固定した。
吉田 勝; 浅野 雅春; 嘉悦 勲; 中井 克幸*; 山中 英寿*; 鈴木 孝憲*; 志田 圭三*; 鈴木 慶二*
Biomaterials, 4, p.33 - 38, 1983/00
被引用回数:17 パーセンタイル:68.39(Engineering, Biomedical)長期間にわたって緩徐な薬物溶出性能をもつ複合体を低温過冷却状態においてガラス化性モノマーの放射線重合によって試作した。複合体からのTSSのin vitro溶出はmatrix-controlled processに従うことが見出された。この場合、drug deliveryの速度は担体の親水性に依存し、含水率が増加するほど増加した。in vivo実験の場合、複合体は30日間の試験期間にわたって去勢したウイスター系ラットの背中の皮下に埋入した。TSSのin vivo速度はin vitroのそれに比べ抑制された。この抑制作用は担体の親水性とよく対応していることが分った。一方、ラットにおける生理学的機能はTSS包含複合体を用いて前立腺腹葉の重量およびserum中の薬物濃度を測定することにより検討した。前立腺腹葉の重量は薬物の溶出速度の増加に伴ない直線的に増加する傾向を示した。またserum中の薬物濃との間にもよい対応関係が認められた。さらに担体自体の生体適合性に関する評価も試みた。
嘉悦 勲; 吉田 勝; 熊倉 稔; 山田 明夫*; 桜井 靖久*
Biomaterials, 1(1), p.17 - 22, 1980/00
被引用回数:16 パーセンタイル:69.27(Engineering, Biomedical)マイトマイシンC,アドリアマイシン,FT-207のような多成分制癌剤を重合物の存在下ガラス化性モノマーの放射線重合によって単一マトリックス中に包括した。各々の制癌剤の溶出挙動はマトリックス中に含まれる三つの制癌剤の組成,含有量によってコントロールできる。そして各制癌剤の溶出速度は吸着剤の添加によって抑制され、pore-making剤の添加によって加速された。一方、MMC ウロキナーゼのように著るしく異なった分子量を有する薬物の溶出についても検討した。この場合二重包括法を用いることにより、両者の薬物の溶出をコントロールできることが判明した。また、マトリックスの構造は電子顕微鏡を用いて検討した。さらに、マトリックスの抗凝血性(thrombogenicity)についても調べた。